Transfert en cours..., vous êtes sur le "nouveau" serveur data.abuledu.org dont l'hébergement est financé par l'association abuledu-fr.org grâce à vos dons et adhésions !
Vous pouvez continuer à soutenir l'association des utilisateurs d'AbulÉdu (abuledu-fr.org) ou l'association ABUL.
Suivez la progression de nos travaux et participez à la communauté via la liste de diffusion.
Votre recherche ...
Nuage de mots clés
Corrosion d'une coque de bateau
Corrosion atmosphérique et biologique de la coque d'un bateau : Les "antifoolings" ne limitent que temporairement la corrosion des coques de bateaux.
Métaux, Photographie, Fours, Métaux -- Surfaces, Corrosion, Métaux -- Analyse, Métaux -- Composition, Métaux -- Défauts, Métaux -- Oxydation anodique, Oxydation, Oxyde ferreux, Physico-chimie
Corrosion par la rouille
Corrosion d'une plaque de four par la rouille. La corrosion désigne l'altération d'un matériau par réaction chimique avec un oxydant (le dioxygène et le cation H+ en majorité). Les exemples les plus connus sont les altérations chimiques des métaux à l'air ou dans l'eau, telle la rouille du fer. L'étude fondamentale des phénomènes de corrosion relève essentiellement de l'électrochimie. L'étude appliquée des phénomènes de corrosion est un domaine de la science des matériaux, qui comporte à la fois des notions de chimie et de physique (physico-chimie). La corrosion est un problème industriel important : le coût de la corrosion, qui recouvre l'ensemble des moyens de lutte contre la corrosion, le remplacement des pièces ou ouvrages corrodés et les conséquences directes et indirectes des accidents dus à la corrosion, est estimé à 2 % du produit brut mondial). Chaque seconde, ce sont quelque 5 tonnes d'acier qui sont ainsi transformées en oxydes de fer…
Métaux, Dessins et plans, Physique, Corrosion, Chimie, Acier inoxydable, Air, Air -- Humidité, Passivation (chimie), Passivité (chimie)
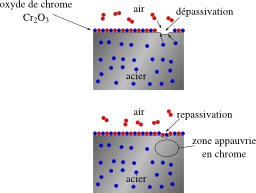
Dépassivation et repassivation de l'inox
Dépassivation (rupture de la couche d'oxyde) et repassivation d'un acier inoxydable : les atomes de chrome dans l'acier réagissent avec le dioxygène de l'air et forment une couche protectrice d'oxyde de chrome. La passivation ou passivité représente un état des métaux ou des alliages dans lequel leur vitesse de corrosion est notablement ralentie par la présence d'un film passif naturel ou artificiel, par rapport à ce qu'elle serait en l'absence de ce film. Dans la plupart des cas (aluminium, acier, acier inoxydable, titane…), ce film passif apparait spontanément par oxydation, parce que l'oxyde formé sur la surface est insoluble et constitue un obstacle qui ralentit les processus ultérieurs. Dans un milieu aqueux, la formation de ce film est liée à un domaine de potentiel électrochimique ainsi qu'à un domaine de pH dans lesquels l'oxyde est stable. De ce fait, on s'attache à ce que le film passif se forme à l'air avant la mise en service de la pièce.
Métaux, Dessins et plans, Protection, Corrosion, Oxyde ferreux, Corrosion électrochimique, Diagrammes, Matériaux résistant à la corrosion, Stabilité
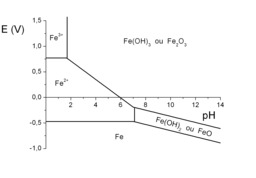
Diagramme potentiel pH du fer
Diagamme potentiel-pH (diagramme de Pourbaix) de l'élément fer à 25°C en milieu aqueux (simplifié). La stabilité du fer dans l'eau dépend : du pH, qui détermine la concentration d'ions H3O+ dans l'eau ; du potentiel électrique de la pièce en fer par rapport à la solution, qui détermine la capacité des électrons à quitter le fer. On peut ainsi tracer un diagramme potentiel-pH (E, pH), en indiquant les zones de stabilité du fer (Fe), les zones de stabilité de l'ion Fe2+ (ou « ion fer II »), les zones de stabilité de l'ion Fe3+ (ou « ion fer III ») et les zones de passivation. Il s'agit donc d'une sorte de « carte », les zones délimitées par des frontières indiquant les couples de valeurs (E, pH) pour lesquelles une espèce est stable. Ce diagramme porte le nom de diagramme de Pourbaix, et peut être tracé pour tous les métaux. Pour savoir si un matériau est adapté à un milieu, il suffit de regarder le diagramme de Pourbaix de ce matériau. Si le couple (E, pH) se situe dans une zone de stabilité, le matériau est protégé contre la corrosion généralisée.
Photographie, Dessins et plans, loup, Lièvres, Bateaux, Grenouilles, Antiquités, Gravure, Peinture, Clip art, Balles et ballons, Amphibiens, Fleurs, Géométrie, Couleurs, Accumulateurs, Piles électriques, Plages, Forêts, Sable, Parasols, Cuisine (pain), Jardinage, Jardins, Réfrigérateurs, Réfrigération et appareils frigorifiques, Bains, Bovins de boucherie, Crustacés, Cuisine -- Appareils et matériel, Nuages, Produits viticoles, feu, Linux (système d'exploitation des ordinateurs), Compas, Salades, Livres illustrés pour enfants, Ombres, laine, Poisson, Plantes des jardins, Confitures, Outillage, Pêches, Cartes à jouer, Mer, Architecture végétale des jardins, Légumes, Potages, Navires à voiles, Découpage (cuisine), Viande, Viande -- Coupe, Étoiles, Cuisine (porc), Saucisses, Enseignes, Tables (meubles), Ongle, Cuisine (aliments naturels), Thé, Bleu, Mouton (viande), soleil, Cuisine (oeufs), Peur chez les animaux, Caricatures et dessins humoristiques, noir, Mécanique, Navires, Triangle, Oeufs, Baies (fruits), Porc, Émotions, Albums à colorier, Nombres cardinaux, Éléments de cuisine, Ustensiles de cuisine, Dinde (viande), Nouvelle-Zélande -- Civilisation, Boissons non alcoolisées, Peur, Pâtisseries, Familles, Fêtes -- Accessoires, Cuisine (fromage), Gelées (confiserie), Maillots de bain, Alimentation, Ciel, Temps -- Systèmes et normes, Oeufs -- Coquilles, Poissons d'eau douce, Parents et enfants, Cuisine (poisson), Véhicules prioritaires, Poulet (viande), Râteaux, Animaux des forêts, Cheminées, Couple -- Psychologie, Espace-temps, Cuisine (sucre), Bains de soleil, Terre, Veaux, Vents, Pyramides, Couple, Graines, Filage à la main, Poissons de mer, Rouge, Aluminium, Vert, Sacs, Membres, Cercle, Navires -- Équipement, Physique, Lumière, Lumière -- Propagation, Joie, Géologie -- Cartes, Poisson rouge, Saumon rouge, Agriculture -- Outillage, Coeur, Art médiéval, Trèfles, Pyramides -- Égypte, Cristaux, Blé, Batteries, Marbre, Fillettes, Caricature, Calcaire, Plantes méditerranéennes, Géométrie euclidienne, Navigation à voile, Cuisine (légumes verts), Sacs en tissu, Pelles, Thalès, Théorème de, Seizième siècle, Dix-neuvième siècle, Dix-septième siècle, Cuivre, Grumes, Albums, Pères, Pères et filles, Sentiers, Maisons individuelles, Pattes, Refus d'obéissance, Jardins médiévaux, Lièvre d'Europe, Méditerranée (région), Cuisine (thym), Aliments crus, Parapente, Vol libre, Dix-huitième siècle, France (Révolution) (1789-1799), Albrecht Dürer (1471-1528), Vinaigre, Poisson fumé, Poisson salé, Auckland (Nouvelle-Zélande), Nouvelle-Zélande (1945-....), Aliments, Cuisine (fruits), Aliments d'origine animale, Aliments fermentés, Cuisine (légumes), Produits de l'oeuf, Boissons alcoolisées, Hérodote (0484?-0420? av. J.-C.), Circulation, Vents -- Vitesse, Métamorphisme (géologie), Savants français, Cuisine (aliments crus), Cuisine (fruits de mer), Cuisine (aliments surgelés), Volaille (viande), Cuisine (poulet), Cuisine (volaille), Produits du blé, Sirops, Sauce à salade, Cuisine (viande), Cuisine (plantes odoriférantes), Crèmes (desserts), Entremets, Poisson surgelé, Agneau (viande), Desserts, Hors-d'oeuvre, Cuisine (baies), Cuisine (vinaigre), Ondes, Cuisine (céréales), Jeux de plage, Conduits d'évacuation de fumées, Fumées, Pull-over, Bronzage, Astérides, Seaux, Serviettes, Chlorure de sodium, Cycle hercynien, Boeuf (viande), Rôtis, Rotissoires, Plats complets, Astacidés, Cuisine (écrevisses), Décapodes (crustacés), Écrevisses, Vinaigrette, Champignons cultivés, Cuisine (champignons), Cuisine (truffes), Truffe du Périgord, Tubéracées, Cassis, Cassissier, Cuisine (cassis), Aliments -- Composition, Blanquette, Cuisine (veau), Veau (viande), Veaux -- Alimentation, Omble de fontaine, Poissonneries, Saumons, Saumons -- Pêche commerciale, Cuisine (semoule), Semoule, Cônes de pin, Pignons (graines), Aliments enrichis, Cuisine (restes), Tourtes, Deux, Jeux de société, Trois, Soupes, Infusions, Lumière, Théorie ondulatoire de la, Cuisson sur réchaud de table, Fondues, Savants allemands, Jumeaux, Interférence (optique), Rhubarbe, Augustin Fresnel (1788 - 1827), Diffraction, Ondes -- Diffraction, Énergie, Photons, Temps, Mesure du, France (Chute des Girondins) ( 30 mai-2 juin 1793), Exécutions capitales et exécuteurs, France (1793), Espace de Minkowski, Relativité (physique), Cônes de lumière, Relativité générale (physique), Architecture égyptienne, Constructions en pierres sèches, Cuisine (rhubarbe), Rhubarbes, Cuisine (boeuf), Cuisines, Aliments -- Consommation, Césium, Horloges à césium, Horloges atomiques, Berne (Suisse), Échelles de temps atomique, Temps (droit international), Johannes Kepler (1571-1630), Des révolutions des orbes célestes - Nicolas Copernic (1473-1543), Héliocentrisme, Énergie éolienne en mer, Portance, Aérodynamique, Relativité restreinte (physique), Muons, Rayons cosmiques, Aquarelle, Le lièvre - Albrecht Dürer (1471-1528), Peintres allemands, Cuisine (plantes aromatiques), Résistance à la chaleur, Thymus (plantes), Abats, Cuisine (abats), Tripes, Aliments -- Réfrigération, Entreposage frigorifique, Frigidaire, Frigo, Danse maorie, Ethnologie -- Nouvelle-Zélande, Linux (logiciels), Rugby, Bayonne (Pyrénées-Atlantiques), Ferias, Aliment, Chevreau (viande), Tacuini sanitatis - al-Muẖtār ibn al-Ḥasan ibn ʿAbdūn ibn Saʿdūn Ibn Buṭlān (10..-1066?), Tangram, Corrosion, Corrosion électrochimique, Assemblages à rivets, Corrosion galvanique, Réactions chimiques -- Mécanismes, Électricité, Symétrie, Constructions géométriques, Génie mécanique, Ressorts et suspension, Ressorts, Volutes, Algues marines, Algues -- Aspect économique, Navires -- Australie, Navires -- Déchets -- Élimination, Navires océanographiques, Navires -- Règlements de sécurité, Sargasses, Mer des, Auteurs arabes, Yuwānīs Ibn Buṭlān (10..-1066?), Jardins -- Aspect symbolique, Famille -- Anthropologie, Famille -- Loisirs, Famille -- Santé et hygiène, Mouton (laine), Quenouilles, Regroupement familial, Veillées, Scènes de la vie quotidienne, Vie quotidienne, Révolution industrielle, Projection cinématographique, Signes et symboles, Carreau, Cartes à jouer, Jeux avec, Pique, Trèfle, Chaleur -- Convection, Dissipateurs thermiques (électronique), Électronique, Acides aminés, Protéines