Transfert en cours..., vous êtes sur le "nouveau" serveur data.abuledu.org dont l'hébergement est financé par l'association abuledu-fr.org grâce à vos dons et adhésions !
Vous pouvez continuer à soutenir l'association des utilisateurs d'AbulÉdu (abuledu-fr.org) ou l'association ABUL.
Suivez la progression de nos travaux et participez à la communauté via la liste de diffusion.
Votre recherche ...
Nuage de mots clés
Métaux, Photographie, Fours, Métaux -- Surfaces, Corrosion, Métaux -- Analyse, Métaux -- Composition, Métaux -- Défauts, Métaux -- Oxydation anodique, Oxydation, Oxyde ferreux, Physico-chimie
Corrosion par la rouille
Corrosion d'une plaque de four par la rouille. La corrosion désigne l'altération d'un matériau par réaction chimique avec un oxydant (le dioxygène et le cation H+ en majorité). Les exemples les plus connus sont les altérations chimiques des métaux à l'air ou dans l'eau, telle la rouille du fer. L'étude fondamentale des phénomènes de corrosion relève essentiellement de l'électrochimie. L'étude appliquée des phénomènes de corrosion est un domaine de la science des matériaux, qui comporte à la fois des notions de chimie et de physique (physico-chimie). La corrosion est un problème industriel important : le coût de la corrosion, qui recouvre l'ensemble des moyens de lutte contre la corrosion, le remplacement des pièces ou ouvrages corrodés et les conséquences directes et indirectes des accidents dus à la corrosion, est estimé à 2 % du produit brut mondial). Chaque seconde, ce sont quelque 5 tonnes d'acier qui sont ainsi transformées en oxydes de fer…
Métaux, Dessins et plans, Protection, Corrosion, Oxyde ferreux, Corrosion électrochimique, Diagrammes, Matériaux résistant à la corrosion, Stabilité
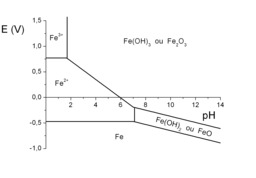
Diagramme potentiel pH du fer
Diagamme potentiel-pH (diagramme de Pourbaix) de l'élément fer à 25°C en milieu aqueux (simplifié). La stabilité du fer dans l'eau dépend : du pH, qui détermine la concentration d'ions H3O+ dans l'eau ; du potentiel électrique de la pièce en fer par rapport à la solution, qui détermine la capacité des électrons à quitter le fer. On peut ainsi tracer un diagramme potentiel-pH (E, pH), en indiquant les zones de stabilité du fer (Fe), les zones de stabilité de l'ion Fe2+ (ou « ion fer II »), les zones de stabilité de l'ion Fe3+ (ou « ion fer III ») et les zones de passivation. Il s'agit donc d'une sorte de « carte », les zones délimitées par des frontières indiquant les couples de valeurs (E, pH) pour lesquelles une espèce est stable. Ce diagramme porte le nom de diagramme de Pourbaix, et peut être tracé pour tous les métaux. Pour savoir si un matériau est adapté à un milieu, il suffit de regarder le diagramme de Pourbaix de ce matériau. Si le couple (E, pH) se situe dans une zone de stabilité, le matériau est protégé contre la corrosion généralisée.