Transfert en cours..., vous êtes sur le "nouveau" serveur data.abuledu.org dont l'hébergement est financé par l'association abuledu-fr.org grâce à vos dons et adhésions !
Vous pouvez continuer à soutenir l'association des utilisateurs d'AbulÉdu (abuledu-fr.org) ou l'association ABUL.
Suivez la progression de nos travaux et participez à la communauté via la liste de diffusion.
Votre recherche ...
Nuage de mots clés
Dessins et plans, Lumière, Lumière -- Propagation, Matière, Ondes électromagnétiques, Absorption, Lumière -- Absorption, Physique nucléaire, Transfert d'énergie
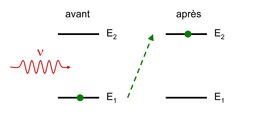
Absorption entre niveaux atomiques
Processus d'interaction entre la lumière et la matière : illustration du phénomène d'absorption entre les niveaux atomiques : Le photon d'énergie h u fait passer l'atome de son état fondamental 1 vers l'état excité 2. Lorsqu'il est éclairé par un rayonnement électromagnétique (la lumière), un atome peut passer d'un état n à un état n' > n, en prélevant l'énergie correspondante sur le rayonnement. Ce processus est résonnant : la fréquence du rayonnement omega doit être proche d'une fréquence de Bohr atomique pour qu'il puisse se produire. Les fréquences de Bohr atomiques sont définies par hbaromega_{nn'}=(E_{n'}-E_n), où E_{n'} > E_n sont les énergies des états n' et n. On peut interpréter ce processus comme l'absorption d'un photon du rayonnement (d'énergie hbaromega=h u) faisant passer l'atome du niveau d'énergie E_n vers le niveau d'énergie E_{n'}. La condition de résonance correspond alors à la conservation de l'énergie.
Photographie, Phares -- France, Ondes, Ondes -- Propagation, Matière, Baleines (Charente-Maritime), Phare des, Énergie de la houle, Houle, Ondes de surface
Houle croisée au phare des baleines
Mer croisée, peu agitée. Petite houle au pie du Phare des Baleines, île de Ré, janvier 2011. La houle est un mouvement ondulatoire de la surface de la mer qui est formé par un champ de vent éloigné de la zone d'observation (vent lointain). C'est donc un cas particulier de vague non déferlante. Il présente un aspect relativement régulier bien qu'il ne corresponde pas à la définition de la vague régulière périodique. Il ressemble plutôt à une telle onde dont l'amplitude varie lentement. Plus précisément c'est la partie de l'état de la mer qui se caractérise par son absence de relation avec le vent local. Une houle se caractérise en première approximation par une hauteur, double de l'amplitude, (de quelques décimètres à quelques mètres) et une longueur d'onde ou une période (généralement de l'ordre d'une dizaine de secondes). En réalité, il s'agit d'un phénomène qui n'est pas périodique et qui peut s'interpréter comme une somme d'une infinité de composantes sinusoïdales infiniment petites.
Dessins et plans, Chaleur de vaporisation, Condensation, Fusion (chimie physique), Gaz -- Liquéfaction, Ionisation, Matière, Métaux -- Solidification rapide, Sublimation (physique), Vaporisation
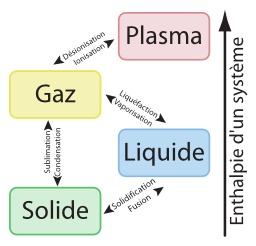
Les états de la matière
Graphique des relation des états de la matière légendé en français : enthalpie d'un système. Les quatre états : plasma, gaz, liquide, solide. Les transformations : solidification / fusion ; sublimation / condensation ; ionisation / désionisation ; liquéfaction / vaporisation.