Transfert en cours..., vous êtes sur le "nouveau" serveur data.abuledu.org dont l'hébergement est financé par l'association abuledu-fr.org grâce à vos dons et adhésions !
Vous pouvez continuer à soutenir l'association des utilisateurs d'AbulÉdu (abuledu-fr.org) ou l'association ABUL.
Suivez la progression de nos travaux et participez à la communauté via la liste de diffusion.
Votre recherche ...
Nuage de mots clés
Assortiment de raccords en cuivre
Assortiment de raccords en cuivre pour plomberie : coude à 45° femelle-femelle, T égal, raccord ; bouchon, coude à 90° femelle-femelle, réducteur, coude à 45° mâle-femelle. Environ 98 % du cuivre est utilisé sous forme métallique, profitant de ses propriétés physiques spécifiques - malléabilité et ductilité, bonne conductivité thermique et électrique et du fait qu’il est résistant à la corrosion. Le cuivre s’avère souvent trop mou pour certaines applications, aussi est-il intégré à de nombreux alliages. On compte parmi ceux-ci le laiton, alliage de cuivre et de zinc ou le bronze, alliage de cuivre et d'étain. On peut usiner le cuivre, bien qu’il soit souvent nécessaire de faire appel à un alliage pour les pièces de forme complexe, comme les pièces filetées, afin de conserver des caractéristiques d’usinabilité satisfaisantes. Sa bonne conductivité thermique permet de l’utiliser pour les radiateurs et les échangeurs de chaleur.
Atome stylisé de lithium
Le lithium est un élément chimique, de symbole Li et de numéro atomique 3. Dans le tableau périodique des éléments, il est situé dans le groupe 1, parmi les métaux alcalins. Comme tous les métaux alcalins, il est très réactif et est généralement conservé dans de l'huile minérale pour le préserver de l'air. Le lithium pur est un métal mou, de couleur blanc argenté, qui se ternit et s'oxyde très rapidement au contact de l'air et de l'eau, prenant une teinte grise virant rapidement à l'anthracite et au noir. C'est l'élément solide le plus léger. Il est essentiellement utilisé pour réaliser des verres et des céramiques réfractaires, des alliages à la fois légers et résistants pour l'aéronautique, et surtout des piles au lithium et des batteries au lithium. Les noyaux des deux isotopes stables du lithium comptent parmi les noyaux atomiques ayant l'énergie de liaison par nucléon la plus faible de tous les isotopes stables, ce qui signifie que ces noyaux sont en fait assez peu stables comparés à ceux des autres éléments légers. C'est pourquoi ils peuvent être utilisés dans des réactions de fission nucléaire comme de fusion nucléaire. C'est également la raison pour laquelle le lithium est moins abondant dans le Système solaire que 25 des 32 éléments chimiques les plus légers. Le lithium joue par conséquent un rôle important en physique nucléaire. La transmutation d'atomes de lithium en tritium a été la première réaction de fusion nucléaire artificielle, et le deutérure de lithium est le combustible de la bombe H.
Photographie, Histoire, Platine, Métrologie, Mètre (unité de longueur), Prototypes, Iridium -- Alliages, Mesures (métrologie)
Barre servant de prototype du mètre jusqu'en 1960
La barre de platine-iridium utilisée comme prototype du mètre (Système International) de 1889 à 1960, image générée par ordinateur : 90% platine et 10% iridium, d'après le standard du "Mètre des Archives". Vingt-neuf copies en furent distribuées.
Dessins et plans, Physique, Câbles sous-marins, Matériaux, Alliages fer-nickel, Laboratoires, Permalloy, Recherche industrielle -- Laboratoires
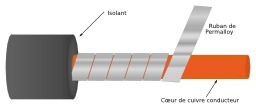
Câble sous-marin en Permalloy
Câble sous-marin atlantique en Permalloy. Source : Permalloy_cable, traduction en français Christophe Catarina. Le Permalloy est un alliage magnétique de fer et de nickel, découvert en 1914 par Gustav Elmen des Laboratoires Bell. Il contient généralement 15 % de fer et 80 % de nickel ; sa désignation symbolique selon la norme européenne est donc NiFe15. Il a une perméabilité magnétique élevée, une coercitivité basse, une magnétostriction proche de zéro et une magnétorésistance anisotropique significative. Les Laboratoires Bell - Bell Telephone Laboratories ou AT&T Bell Laboratories - , plus connus sous l'appellation de Bell Labs), furent fondés en 1925 et implantés à Murray Hill dans l'État américain du New Jersey. En 2009, ils font partie du centre de recherche et développement d'Alcatel-Lucent. Ils ont déposé plus de 25 000 brevets et en déposent actuellement 3 nouveaux chaque jour. Les recherches menées aux laboratoires Bell ont eu une importance capitale dans des domaines tels que les télécommunications (réseau téléphonique, transmission télévisuelle, communications satellite, etc.) et l'informatique (transistor, Unix, C et C++, etc.). Ce sont des laboratoires Bell que proviennent aussi la cellule photoélectrique et le laser et l'extraordinaire développement des communications par fibre optique.
Cristaux d'Osmium
Cristaux d'Osmium (Os), cristallisé produit par réaction de transport chimique dans une atmosphère de chlore. Masse : 2,2 g, pureté ≥ 99.99%. L’osmium est l'élément chimique du tableau périodique dont le symbole est Os et le numéro atomique 76. Il se présente sous la forme d'un métal gris bleuté et brillant. C'est un métal de transition appartenant aux métaux du groupe du platine. Il est l'élément naturel le plus dense sur Terre. Il est le plus souvent trouvé nativement en alliage avec le platine ou l'iridium. Les alliages d'osmium sont employés notamment dans les pointes de stylo plume, les contacts électriques et dans d'autres applications où sa dureté et sa résistance extrêmes sont requises.
Métaux, Dessins et plans, Physique, Corrosion, Chimie, Acier inoxydable, Air, Air -- Humidité, Passivation (chimie), Passivité (chimie)
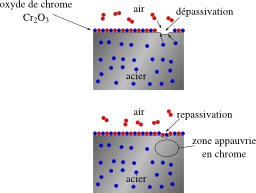
Dépassivation et repassivation de l'inox
Dépassivation (rupture de la couche d'oxyde) et repassivation d'un acier inoxydable : les atomes de chrome dans l'acier réagissent avec le dioxygène de l'air et forment une couche protectrice d'oxyde de chrome. La passivation ou passivité représente un état des métaux ou des alliages dans lequel leur vitesse de corrosion est notablement ralentie par la présence d'un film passif naturel ou artificiel, par rapport à ce qu'elle serait en l'absence de ce film. Dans la plupart des cas (aluminium, acier, acier inoxydable, titane…), ce film passif apparait spontanément par oxydation, parce que l'oxyde formé sur la surface est insoluble et constitue un obstacle qui ralentit les processus ultérieurs. Dans un milieu aqueux, la formation de ce film est liée à un domaine de potentiel électrochimique ainsi qu'à un domaine de pH dans lesquels l'oxyde est stable. De ce fait, on s'attache à ce que le film passif se forme à l'air avant la mise en service de la pièce.
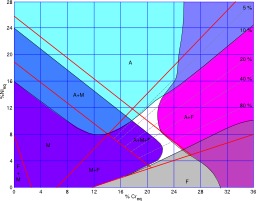
Diagramme de Schaeffler pour la soudure
Diagramme de Schaeffler pour la soudure des aciers inoxydables. A : austénite γ ; F : ferrite α ; M : martensite ; 5-80% : pourcentage en masse de la ferrite dans l'austénite ; zones de risques : bleu clair, fissuration à chaud ; violet, fissuration à froid ; rose, fragilisation par transformation α→σ ; gris, fragilisation par croissance des grains α ; blanc, zone idéale. L'acier inoxydable, couramment appelé acier inox ou inox, a un grand rôle dans d'innombrables domaines : vie quotidienne, industries mécaniques, agroalimentaires, chimiques, transports, médecine, chirurgie, etc. C'est une famille d'aciers, alliages de fer et de carbone, auxquels on ajoute essentiellement du chrome qui, au-delà de 10,5 % en solution (selon la teneur en carbone) dans la matrice, provoque la formation d'une couche protectrice d'oxyde de chrome qui confère à ces aciers leur inoxydabilité.
Disque de Vanadium
Disque de Vanadium (pureté : 99,95 %) obtenu à l'aide de la fusion par faisceau d’électron, usiné par Électro-érosion, poli, puis gravé à l'acide. Taille : 35 mm de diamètre, masse : 31,5 g environ. Le vanadium est un élément chimique, de symbole V et de numéro atomique 23. C'est un métal rare, mou et ductile que l'on trouve dans certains minerais. Il est principalement utilisé dans les alliages.
Fragements purs (99,9 %) de cobalt
Le cobalt est un élément chimique, de symbole Co, de numéro atomique 27 et de masse atomique 59. Il est utilisé en métallurgie (33 %) pour les superalliages (22 %) et les alliages durs (11 %). Une part importante (22 %) est utilisée dans la fabrication d'accumulateurs, secteur en pleine évolution et une autre (7 %) dans la fabrication d'aimants. Le cobalt est également utilisé dans des secteurs non-métallurgiques comme la catalyse (11 %), les pigments (9 %), les pneus, les colles, les savons... La production mondiale de cobalt en 2006 était de 55 000 tonnes8. La chimie du cobalt en solution aqueuse et la formation de complexes est particulièrement riche.
Métaux, Dessins et plans, Cuivre, Alliages métalliques, Matériaux, Cuivre -- Alliages, Dessin hachuré
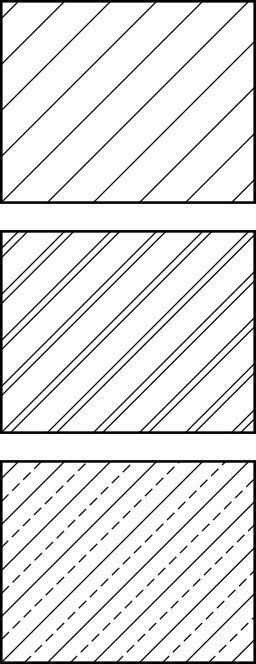
Hachures de représentation des métaux
Hachures utilisées généralement sur les plans d'ensemble pour représenter les pièces métalliques coupées : tout métal (haut), alliages légers (alliages d'aluminium, de magnésium : milieu), alliages de cuivre (cuivre, bronze, laiton : bas).
Louche
Louche (London Hallmark 1876-77 & initiales FH). Le mot louche est apparu au XIIIe siècle, dérivé de "louce" mot de la langue francique, mais on a continué encore longtemps à l'appeler "cuillère à pot" qui désignait une grosse louche. En ce qui concerne sa capacité, elle est généralement située entre la cuillère et le bol, et bien qu'il n'y ait pas de mesure précise, la louche traditionnelle contient un quart de litre mais les louches actuelles sont souvent beaucoup plus petites. D'abord en fer battu étamé, en étain, ou en argent, puis en fer émaillé, en aluminium, en inox, même en verre pour servir les desserts, en plastique.
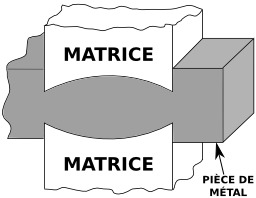
Matriçage d'une pièce de métal
Matriçage d'une pièce de métal. Traduction en français Cyrille Largillier. La forge par matriçage consiste à former par déformation plastique après chauffage des pièces brutes réalisées en alliages non ferreux tels que les alliages d'aluminium, de cuivre, de titane, de nickel, etc. Le matriçage est une opération de forge effectuée à l'aide d'outillage appelés des matrices (demi-matrice supérieure et demi-matrice inférieure). Les matrices portent en creux la forme de la pièce.
Modèle en bois pour moulage au sable
Modèle en bois, résine, ou alliages métalliques monté sur plaques-modèle : coupé en deux et chaque partie est fixée sur une plaque comportant des dispositifs de positionnement. Ce type de modèle s'utilise avec des châssis, comportant les mêmes dispositifs de positionnement, destinés à contenir le sable et à le maintenir lors des manipulations du moule et de la coulée (sable noir). Les entraxes des châssis et des plaques-modèle ne sont pas normalisés, chaque fonderie ayant ses propres standards.
Pointe fondue d'une électrode sacrificielle d'hafnium pur à 99,98 %
Le hafnium est un élément chimique du tableau périodique de symbole Hf et de numéro atomique 72. C'est un métal de transition tétravalent d'un aspect gris argenté. Le hafnium ressemble chimiquement au zirconium et est trouvé dans le minerai de zirconium. Le hafnium est utilisé dans les alliages de tungstène pour la confection de filament et d'électrode, il est aussi utilisé comme absorbeur de neutrons dans les barres (ou croix) de contrôle de la réactivité nucléaire.
Statue d'Arlequin
Statue en plomb d'Arlequin, Wrest Park, Silsoe, Bedfordshire : attribuée à l'atelier de John Cheere entre 1740 et 1787.
Trois barres de vanadium cristallisé pur à 99,9 %
Le vanadium est un élément chimique, de symbole V et de numéro atomique 23. C'est un métal rare, dur et ductile que l'on trouve dans certains minerais. Il est principalement utilisé dans les alliages.